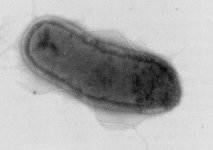
براي اولين بار در سال 1907 افرادي بنام هاي Townsend, Smith عامل بيماري گال را در گياهان جداسازي وشناسايي نمودند و به نام polymonastumefaciens معرفي گرديد. در سال 1942 اين نام توسط Connبه Agrobacteriumtumefaciens تغيير يافت. (Agros =زمين و مزرعه و bakterion=ميله اي شكل كوچك )
توصيف جنس Agrobacterium
باكتري هاي متعلق به اين جنس معمولا"ميله اي شكل در ابعاد 1.5-3 * 0.6-1 ، فاقد اسپور ، گرم منفي ، متحرك با يك تا 6تاژك محيطي بوده كه يك تا 2 تاي آن ممكن است نزديك به قطبي باشند و اندازه تاژك ها4 تا 5 برابر اندازه طول سلول باكتري است.
اين باكتري ها هوازي ، داراي متابوليسم تنفسي(با اكسيژن بعنوان گيرنده نهايي الكترون) بوده ، بعضي استرين هاقادر به رشد ( بي هوازي ) در حضور نيترات مي باشند . درجه حرارت اپتيمم 25 تا 28 درجه و PHمناسب 6 تا 7 است. كلني ها مدور ، برجسته ، صاف و بيرنگ تا بژ بوده و رشد روي محيطهاي حاوي قند غالبا" با توليد پلي ساكاريد خارج سلولي فراوان همراه است.
باكتري هاي متعلق به اين جنس كاتالاز واوره آز مثبت بوده، بعضي استرين ها 3-ketoglycoside ها را توليد مي كنند. كموارگانوتروف بوده و از طيف وسيعي از كربوهیداتها ، اسيدهاي آلي ، و آمينواسيدها بعنوان منبع كربن استفاده مي كنند ولي قادر به استفاده از سلولز نيستند. در محيط هاي پايه معدني از قند هاي گلوكز ، گالاكتوز و ديگر كاربوئيدراتها اسيد توليد ميكنند. بعضياز استرينها از نمك هاي آمونيوم و نيترات بعنوان منبع Nاستفاده ميكنند و بعضي استرينها نياز به عوامل رشد دارند.
بعضي استرينهاي اين جنس به طوقه ،ريشه و ساقه ي تعداد زيادي از گياهان دولپه و بازدانه حمله كرده و سلولها را تبديل به سلولهاي سرطاني با رشد خارق العاده مي نمايند. بيماريهاي ايجاد شده شامل گال طوقه ، ريشه مويي است.
توليد گال توام است با وجود يك پلازميد بزرگ (Ti) و توليد ريشه زياد با پلازميد بزرگ Ri .
ميزان G+C در DNA بين 58 تا 62 درصد است.
اين باكتري ها به عنوان باكتري هاي مولد تمور ، گال و يا ريشه هاي انبوه موئين ، چون ديگر باكتري هاي ساكن خاك ميتوانند سال هاي متمادي در ريزوسفر گياهان و حتي طبق برخي گزارش ها در خاك هايمزارع گوجه فرگي و پنبه با 5 سال سابقه عدم كاشت ادامه بقا بدهند.
طبقه بندي باكتري هاي متعلق به اين جنس
شناسايي و طبقه بندي اين گروه از باكتري ها بيشتر براساس صفات و رفتار بيماريزايي آنهاست وصفات بيوشيميايي ، فيزيولوژيكي و غيره كمتر به عنوان محك اصلي در تفكيك گونه ها و طبقه بندي هاي مربوطه مورد استفاده قرار گرفته است. در همين راستا اگروباكتريوم ها به چهار گروه يا گونه ( پاتوار ) تقسيم مي شوند :
1. استرين هايي كه ايجاد سرطان طوقه يا تمور مي نمايند و جزوگونة A. tumefaciensبه شمار مي آيند. اين استرين ها به دليل پلي فاژبودن (polyphage) داراي دامنه بسيار وسيع ميزباني بوده و به نوبة خود براساس صفات بيوشيميايي و فيزيولوژيكي به دو بيووار 1 و 2 تقسيم مي شوند. بيووار 3 اين باكتري ( استرين هاي انگور ) در طبقه بندي جديد مستقلا" تشكيل گونة جديدي به نام A. vitis داده است.
- استرين هايي كه ايجاد ريشه هاي موئين در ميزبان هايي چون سيب ، گلابي ، تمشك ، رز مي نمايند و جزو گونه A. rhizogenes قرار مي گيرند صرفا" داراي يك بيووار مي باشند.
- استرين هايي كه ايجاد گال ساقه روي انواع تمشك و گل داوودي و انگور مي كنند جزو گونه A.rubi به شمار مي آيند و تاكنون سه استرين براي اين گونة باكتريايي معرفي شده است.
- استرين هايي كه به طور كلي غيربيماريزا مي باشند در گونة A. rabiobacter بادو بيووار قرار دارند. يكي از معايب طبقه بندي فوق عدم ثبات نامگذاري به دليل اتكاي كامل به صفت و رفتار بيماريزايي استرين ها مي باشد و چون ژن هاي مسئول بيماريزايي در اين باكتري ها روي پلاسميدهاي Ti ( پلاسميد مولد تمور ) و Ri ( پلاسميد مولد ريشه ) قرار دارند و كروموزوم يا DNA باكتري نقشي چندان در بيماريزايي ندارد و باتوجه به اينكه پلاسميد به عنوان كروموزم مازاد سلولي نقش حياتي در سلول باكتري ايفاء نمي نمايد و ممكنست به طور طبيعي يا تكرار كشت آزمايشگاهي از بين برود يا به استرين هاي غيربيماريزاي جنس Agrobacterium يا جنس هاي ديگر باكتريايي منتقل شود و سرانجام آنها را تبديل به استرين هاي بيماريزا نمايد ، از اينرو مجموعة اين عوامل موجب شده است تفكيك گونه ها و نامگذاري آنها در شرايط فعلي به صورت يك امر غيرپايدار باقي بماند. در اين راستا آزمون استفاده از آرژنين و دو مشتق آن به نام هاي octopine و nopaline به عنوان منابع نيتروژني و كربن مورد استفاده توسط 95 % يا بيشتر استرين هاي بيماريزا كه به عنوان محك تفكيك استرين هاي بيماريزا از غيربيماريزا مطرح شده است داراي همان نقطة ضعفي مي باشد كه در بالا بدان اشاره شد و آن پلاسميد زاد بودن صفت استفاده از منابع انرژي فوق است.
در سال 1992 Sawada و همكاران براساس آناليزتوالي بارهاي آلي ژن 16srRNA 7 استرين از Ag. و 8 استرينريزوبيوم و ( 3.Ag. بيووار + A. rubi ) را مطالعه كردند. براساس DNAهمولوژي استرين هاي بيووار 1 بنام A. radio ، بيووار 2 بنام A. rhizo و بيووار 3 هم بنام A. vitis و A. rubiپيشنهاد شدند و سپس نام A. tumefaciensرد شد.
علت :
( International Code ofNomenclature of Bacteria) ICNB طبق قانون نامگذاري بايستي يكي از گونه را حذف كنند و بايستي نامي كه اول توصيف شده بماند.
نحوه جداسازي باكتريهاي جنس Agrobacterium
در جداسازي استرين هاي A. rumefaciensداشتن برخي از اطلاعات اوليه داراي اهميت بسيار ميباشد از آن جمله :
1. گال حاصل از A.tumefaciensنسبتا" نرم و به راحتي از ديگر برآمدگي هاي سفت و چوبي گياهي قابل تميزميباشد. نرمي بافت گال سبب ميشود ساپروفيت هاي زيادي در آنها رشد و تكثير يابند وبتدريج بافت گال از بيرون حالت چوب پنبه اي و از درون حالت چوبي پيدا كند.
- همراه گال هيچگونه تراوش هاي باكتريايي توليد نميشود.
- در بافت گال جمعيت سلول باكتري به تعداد انبوه وجود ندارد. بنابراين سوسپانسيوني كه از بافت گياهي تهيه ميشود بسيار روشن و غيركدر است.
- ضدعفوني بافت گال با محلول 1 % سديم هيپركلريت به مدت 20-10 دقيقه قبل از تهيه سوسپانسيون ضروري است و در انتخاب قطعات كوچك بافت ( 1 ميلي متر مربع ) براي تهيه سوسپانسيون حتما" از قسمت هاي سالم نمونه برداري شود زيرا بافت هاي مرده منبع اصلي آلودگي به ساپروفيت هاست.
- كشت باكتري ترجيحا" در محيط كشت هاي اختصاصي انجام پذيرد . در اين محيط كشت ها و محيط كشت هاي عمومي عموما" از مانيتول به عنوان منبع كربني و نيترات سديم به عنوان منبع نيتروژني استفاده ميشود زيرا براي رشد مطلوب استرين هاي Agrobacteria اين منابع كربن و نيتروژن بسيار موثر است. البته نيازمندي هاي رشدي براي بيووارهاي اين استرين ها متفاوت است. به طول مثال برخي استرين هاي بيووار A. tumefaciens و A. rhizogenes نيازمند Biotin يا glutamic acid يا هر دو ميباشند و نيازمندي A. rubi بيشتر به مواد L-glutamic acid و yeast extract است.
- محيط كشت هاي اختصاصي توصيه شده براي اين استرين ها درحال حاضر عبارتند از محيط كشت Brisbane & Kerr medium 1A براي كشت استرين هاي بيووار ، محيط كشت 2E براي كشت استرين هاي بيووار 2 و محيط كشت Roy-Sasser براي كشت استرين هاي بيووار (A. vitis) .
- گاهي در محيط كشت هاي اختصاصي مشكل عدم رشد استرين هاي مذكور به وجود مي آيد. در اينگونه موارد استفاده از محيط كشت NA + % 01/0 yeast extract توصيه ميشود.
- درصورتي كه جداسازي باكتري مستقيما" از گال بر روي محيط كشت هاي ياد شده مقدور نباشد پيشنهاد ميشود كه مقداري بافت گال را كاملا" در آب مقطر استريل له نموده و با عصاره حاصله ميزبان اصلي يا گياه حساس را از طريق زخم يا تزريق آلوده كرده و پس از پيدايش دوباره علائم بيماري در ميزبان تلقيح شده ، نسبت به جداسازي باكتري مولدگال اقدام كرد.
- درصورتي كه با هيچيك از روش هاي فوق باكتري از بافت گال جدا نگرديد يكي از دلايل عدم جداسازي ميتواند عدم وجود باكتري مولدگال باشد زيرا بر طبق گزارش ها ضرورت حضور فيزيكي باكتري در بافت آلوده فقط 3 روز است و به محض انتقال قسمتي از پلاسميد Ti باكتري به سلول گياهي و تركيب آن با DNA هسته سلول گياهي ، خود به خود گياه شروع به تقسيمات سلولي غيرقابل كنترل و سنتزاپين ها ميكند كه اين مواد شيميايي كاملا" اختصاصي صرفا" توسط آن دسته از باكتري هاي A. tumefaciens مورد استفاده قرار ميگيرد كه داراي پلاسميد Ti ميباشند و البته تشكيل گال نيز براي محافظت سلول باكتريايي به كار گرفته ميشود . به اين سيستم پارازيته كردن گياه ، كلني زاسين ژنتيكي گفته ميشود. دليل دوم براي عدم جداسازي ممكنست حضور باكتري در سطح بافت و نه در درون بافت گال باشد در آن صورت استفاده از محيط كشت اختصاصي و دوري كردن از ضدعفوني سطحي گال ، ضروري است.
- درصورتي كه خواسته باشيم اين باكتري ها مستقيما" از خاك جداسازي بشوند لازم است كه حداقل ميزان جمعيت آنها در هر گرم خاك cfu 10[SUP]3[/SUP]باشد ، زيرا وجود جمعيت پايين اين باكتري ها به منزله افزوني جمعيت باكتري هاي ديگر خاك ميباشد. و چون در مرحله جداسازي به دليل حساسيت باكتري به محيط كشت هاي اختصاصي ميزان رشد كلني هاي Agrobateria كاهش مي يابد، روش مناسب كشت بدين سان ميباشد كه مقدار ml 1/0 از عصاره خاك ( 1 گرم در ml 10 آب مقطر ) به كمك پي پت به پتري هاي حاوي محيط كشت هاي مربوطه افزوده و با ميله شيشه اي به شكل L پخش ميشود. پس از پيدايش كلني ها، تك كلني هاي مشكوك به Agrobacterium براي خالص سازي و تفكيك بيشتر استرين ها روي محيط كشت هايي مانند PDA ، NBYES, YDCكشت ميشوند. مضافا" براينكه در جهت تفكيك استرين ها از هم ، روش هاي مطمئن تري چون آزمون بيماريزايي ، آزمون مولد ريشه درديسك هاي هويج ، قدرت استفاده از opines و حساسيت به اگروسين 84 و بالاخره آناليز اسيدهاي چرب ، استفاده از منابع كربني و پروب هاي T-DNA وجود دارند.
چگونگي تهيه محيط كشت هاي اختصاصي
1. محيط كشت IA : (براي جداسازي بيووار 1 A. tumefaciens )
آرابيتول (L-) 04/3گرم
نيترات آمونيم 16/0گرم
KH[SUB]2[/SUB]PO[SUB]4[/SUB] 54/0 گرم
K[SUB]2[/SUB]HPO[SUB]4[/SUB] 04/1گرم
Sodiumtaurocholate 29/0گرم
سولفات منيزيم 25/0گرم
آگار 15 گرم
كريستال ويوله (1/0 درصد) 2ميل
Actidione(2%) 1 ميل
Sodiumselenite (1%) 1ميل
آب مقطر 1 ليتر
2. محيط كشت 2E : (مخصوص جداسازي بيووار2 A. trumfaciens)
نتيرات آمونيم 16/0گرم
Erythritol 05/3 گرم
KH[SUB]2[/SUB]PO[SUB]4[/SUB] 54/0 گرم
K[SUB]2[/SUB]HPO[SUB]4[/SUB] 04/1 گرم
سولفات منيزيم 25/0گرم
Sod.taurocholate 29/0 گرم
آگار 15 گرم
Yeast extract (1%) 1ميل
مالاشيت سبز (%1/0) 5ميل
actidione(2%) 1ميل
Sod.selinite (1%) 1ميل
آب مقطر 1 ليتر
3. محيط كشت Roy-sasser : (مربوط به جداسازي A. vitis)
سولفات منيزيم 2/0گرم
K[SUB]2[/SUB]HPO[SUB]4[/SUB] 9/0 گرم
KH[SUB]2[/SUB]PO[SUB]4[/SUB] 7/0 گرم
adonitol 4 گرم
yeast xtract 14/0گرم
NaC1 2/0 گرم
H[SUB]3[/SUB]BO[SUB]3[/SUB] 1 گرم
Agar 15گرم
Chlorothalonia(Bravo500) (4%) 5/0 گرم
آب مقطر 1 ليتر
پس از تنظيم PH محيط كشت پايه به 2/7 واتوكلاو آن ، در شرايط نيمه گرم مواد زير به صورت مجزا و به طور استريل به محيط كشت فوق اضافه ميشود :
TIC 80 ميلي گرم
D-Cycloserine 20ميلي گرم
Trimethoprim (دريك قطره HCl) 20 ميلي گرم
كلني هاي A.vitis با وسط قرمز تيره باحاشيه سفيد در سطح محيط كشت ظاهر مي شوند.
4. محيط كشت نيمه اختصاصي Clark : (براي جداسازي گونه هاي مختلف)
لاكتور 5گرم
نيترات پتاسيم 1گرم
سولفات منيزيم 1/0گرم
Na[SUB]2[/SUB]HPO[SUB]4[/SUB] 18/0گرم
آگار Oxoid (شماره 3) 12گرم
آب مقطر 1 ليتر
پس از تنظيم PH در 8/6 و آتوكلاو محيط كشت ،مواد زير به طور مجزا و استريل در شرايط نيم گرم به محيط كشت فوق اضافه ميشود.
Ferricsod.sequestrate (25/0 درصد) 1ميل
MnSO[SUB]4[/SUB].4H[SUB]2[/SUB]O (5/33 درصد) 1ميل
در سطح محيط كشت كلني هاي اين باكتري ها به حالت گنبدي شكل سفيد ظاهر ميشوند.
-مكانيسم بيماريزاي Agrobacterium:
اين باكتري در سال 1907 شناخته شد وليمكانيسم بيماريزايي آن تا سال 1970 معلوم نبود. در سال 1974 ، قابليت توليد گال دراسترين حاوي Agrobacteriumمورد مطالعه قرار گرفت و معلوم د كه عامل آن Ti-plasmid نام دارد كه 200kbp وزن دارد و باحذف اين پلاسميد ، باكتري خاصيت بيماريزايي خود را از دست ميدهد. و اين پلاسميداطلاعات لازم براي تكثير و بيماريزايي ، هيپرتروني و هيپر پلاسي را دارد. علاوه براين حاوي ژنهايي است كه ميتواند اپين ها را توليد كند و از آنها بعنوان منبع كربناستفاده ميكنند. Nopalin , octopine , agrocinopine
Le plasmide pTi
- Ti-plasmid داراي دو ناحية مهم از نظر بيماريزايي است :
1. ناحيه T-DNA : قسمتي ازپلاسميد كه به كروموزوم گياه متصل ميشود T-DNA ميگويند.
2. (virulence region)vir region
اين دو ناحيه براي بيماريزايي و توليدگال ضروري است. چيزي كه منتقل ميشود T-DNA است و ناحية vir كار انتقال را انجام ميدهد.
ساير بخش هاي Ti plasmid :
1. ناحية Replication: براي تكثير پلاسميد لازم است و در بيماريزايي نقش ندارد.
2. ناحية conjugation: كار الحاق را انجام ميدهد و انتقال كل پلاسميد را برعهده دارد.
3. ناحية opine catabolism ميتواند اوپين را مصرف كند.
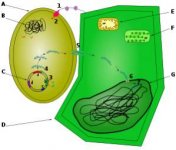
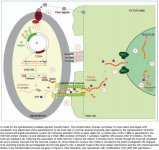
همانطور كه گفته شد : روي پلاسميد ،دو مجموعه ژني وجود دارد كه درمكانيسم بيماريزايي دخالت دارند - ژنهاي روي T-DNA كه به كروموزوم گياه ملحق مي شوند. - ژنهاي ناحيه virulenceكه در انتقال T-DNAبه داخل سلول گياه نقش دارند ولي خودشان منتقل نميشوند.
- T-DNA :
قسمتي از پلاسميد كه با دومرز (Right borderو (left border مشخص ميشود و حدود 24bp است. اين ناحيهحاوي 2 گروه از ژنهاست .
1. oncogenes : ژنهايي كه بيان آن موجب ساختن پروتئينهاي موردنياز در سنتز هورمونهايي مثل ايندول اسينك و اسيد (IAA) و سيتوكيني نميشود و هيپرتروني و هيپرپلاسي و توليد گال ميشود.
2. opine synthetase: اينها سنتز اوپين ها را كد ميكنند و سپس بعنوان منبع كربن و ازت به مصرف باكتري ميرسد. هريك از نژادها اپين خاصي توليد و مصرف ميكنند.
- ناحيه virulence :
با وزن 35bp و معمولا"شامل 8 اپرون است كه بصورت vir A ، vir B، vir C، vir D، vir E، vir F، vir H، vir Gنشان داده ميشوند. بعضي مثل نوپالين ، ممكن است vir Hيا vir Fرا نداشته باشند و بعضي هر 8 اپرون را دارند.
- بيماريزايي :
تركيبات فنلي ساخته شده بوسيله سلولهاي زخمي گياه ميزبان مثل استوسيرينگون Acetosyringon يا كامئبك اسيد ، sinapimic acid باعث فعال شدن ژنهاي ناحيه ويرولانس ميشوند.وجود زخم ضروري است و باعث جلب باكتري و چسبيدن آن به سلول ميزبان ميشوند كه T-DNA توسط ناحيه vir انتقال پيدا ميكند. مراحل دخالت ژنهاي ويرولانسدر بيماريزايي عبارتند از :
1. تشخيص گياه ميزبان ، chomotaxis: تركيبات فنلي ترشح شده توسط ميزبان باعث تحريك ژنها و نيز حركت باكتري به جهت تركيبات ميشود.
2. چسبيدن به سلول گياه ميزبان در دومرحله صورت ميگيرد. 1ـ اتصال ضعيف اوليه 2ـ اتصال قوي باكتري به سلول ميزبان دراثر توليد فيبر هاي سلولزي توسط باكتري در محل اتصال به ميزبان . ژنهاي chvA، chvB، pscAو att در باكتري در اين پروسه نقش دارند.
3. انتقال T-DNA و اتصال به ژنوم گياه ميزبان.
سه مرحله اول احتياج به سلول زخم شده گياه ميزبان دارد.ژنهاي virA و virG مسئول جلب و حركت باكتري بطرف سلولزخم شده گياه ميزبان (virA) و فعال شدن بقيه ژنهاي vir ميشوند.
Organization of the vir region of Tiplasmids
| function | vir locus |
| Regulatory (recognizes plant metabolites, activates virG) | A |
| Regulatory (transcriptional activator of other vir loci) | G |
| Nicks Ti plasmid at T-DNA borders, covalently attaches to “T-strand” | D |
| Unknown function involved in host-range determination | C |
| Ss-DNA binding protein (stabilizes T-DNA during or after transfer) | E |
| Transfer apparatus | B |
| Vir Genes and their Function | � |
| Vir Gene | Function |
| Vir A, Vir G | Sense phenolic compounds from wounded plant cells and induceex pression of other virulence genes |
| VirD2 | Endonuclease; cuts T-DNA at right border to initiate T-strand synthesis |
| Vir D1 | Topiosomerase; Helps Vir D2 to recognise and cleave within the 25bp border sequence |
| Vir D2 | Covalently attaches to the 5I end of the T-strand, thus forming the T-DNA Complex. Also guides the T-DNA complex through the nuclear pores |
| Vir C | Binds to the 'overdrive' region to promote high efficiency T-strand Synthesis |
| Vir E2 | Binds to T-strand protecting it from nuclease attack, and intercalates with lipids to form channels in the plant membranes through which the T-complex passes |
| Vir E1 | Acts as a chaperone which stabilises Vir E2 in the Agrobacterium |
| Vir B & Vir D4 | Assemble into a secretion system which spans the inner and outerbacterialmembranes. Required for Export of the T-complex and Vir E2 into the plant cell |
VirA : پروتئيني ميسازد كه اين پروتئين نقش سنسور يا گيرنده شرايط محيطي را ايفاد ميكند (sensori membrane protein) و اندازه آن حدود 2kb است ( RP پروتئين كدميكند كه به تغيير شرايط حساس است ) وقتي گياه زخمي ميشود و مواد فنله _ قندها _اسيدهاي آمينه و برخي مواد ويژه از جمله acetosyringone به بيرون ترشح ميشود VirA فعال شده و با فعال شدن VirA محصولآن روي virGتاثير ميگذارد و اين ژن فعاليت خودش را شروع ميكند در اثر فعال شدن اين ژن محصولي بوجود مي آيد كه اين محصول به ناحيه T-box مي چسبد و آنها را وادار به فعاليت كند. اگردر ناحية virA، virB، virDو virGموتاسيون صورت گيرد . تومور ايجاد خواهد شد ، اگر در ناحية virC ، virHو virF موتاسيون صورت گيرد باعث محدود شدن دامنة ميزباني و كم شدن خاصيت بيماريزايي ميشود.
virB: كه اندازه آن حدود 9 kb است و شامل 11 ژن ( بزرگترين اپرون ) در اثرفعال شدن آنها ناحيه virBپروتئينهايي توليد ميشود كه در ساختن ساختمان pili در ديواره باكتري فعاليت كرده و مجموعا" يك كانال توخالي مرتبط با بيرون سلول باكتري ايجاد ميكند.
VirD: وقتي فعال ميشود 4 ژن دارد كه ژنهاي اين ناحيه آنزيم هايي را كد ميكند كه خاصيت نوكئازي دارند و ميتوانند به مرزهاي چپ وراست ناحيه DNAT.بچسبند و در اثر اين چسبيدن DNAشكسته و جدا ميشود.
virD: پروتئيني توليد ميكند كه به انتهاي رشتة T-strand از طرف 5` متصل ميشود وكار محافظت از آنزيم نوكلئاز را برعهده دارد.
Virc : ژن در اين ناحيه پروتئين هايي را كد ميكند كه در شناسايي محل برش بر روي رشته T.DNAبه محصولات ژن virDكمك ميكنند.
بعد از اينكه اين رشته از DNAجدا شد ژن virEپروتئيني را كد ميكند كه پروتئين پوششي DNA است تمايل زيادي به اتصال به ssDNAدارد اينها به اين رشته جدا شده T-DNA مي چسبند و حالت پوششي به آن ميدهند و آنرا از آسيب آنزيم هاي نوكلئاز در امان نگه مي دارند. (T-complex) ضمنا" رشته برش خورده را بسمت كانالي كه درديواره ايجاد شده هدايت ميكند و چون سلول باكتري در تماس با سلول زخمي گياه است ،از باكتري خارج و وارد سلول گياه ميشود و در ناحيه اي از كروموزوم گياه كه تصادفي هم هست اين رشته مي چسبد و در كروموزدم گياه ادغام ميشود.
دراين مقطع گياه آلوده بخشي از ژنومباكتري كه ادغام شده جزو ژن هاي خود مي پذيرد. از آنجا كه در روي اين بخش منتقل شده ژن هاي شركت كننده در بيوسنتز هورمون هاي گياهي وبيوسنتزاپين ها قرار گرفتند. لذابا بيان اين ژن ها در اثر بهم خوردن تعادل هورموني گياه ، سلول هاي آلوده به طورمرتب تكثير شده و يك بافت تمايز نيافته ( گل ) را ايجاد ميكنند.
ضمنا" از آنجا كه بخش انتقال يافته حامل ژن هاي توليد مواد اپيني هم هست ، اين مواد هم توليد شده و به بيرون ازگياه ترشح ميشوند و باكتري از اين مواد ترشح شده بعنوان منبع كربن و منبع انرژي استفاده ميكند و به زندگي خود ادامه مي دهد.
در آزمايش ژن virD را از آگروباكتريوم به پلاسميد ديگري كه بيماريزا نيست منتقل كردند و ديدند كه در پلاسميد جديد كه فقطvirDدارد. در استريني كه اين پلاسميد در آنجا قرارگرفته ،piliايجاد شده است و باكتري توانايي conjugationرا داشته پس نقش virDدر tronsformationدخالت ميكند.
از جمله عوامل تعيين كننده دامنه ميزباني در آگروباكتريوم محصول ژن virFاست و نيز محصول virA.چون virAتابع شرايط محيط است و ممكن است مواد فنله كه از سلول هاي زخمي يك گياه خاص ترشح ميشوند قادر به تحريك virAنباشد چون محصول ژن قادر به دريافت آنها نيست. virFبه virA در اين امر كمك ميكند. virGنيز در اين رابطه نقشي را ايفاء ميكند.
كنترل بيولوژيكي crowngall:
كنترل بيولوژيكي بيماري گال طوقه بصورت تجاري صورت ميگيرد و از سال 1973 با استفاده از استرين k-84از A. radiobacter در مورد هسته داران مثل زردآلو و گيلاس و ...بكار ميرود كه توليد باكتربوسيني بنام Agrocine ميكند. باكتريوسين توسط نژادها نزديك گونه بوجود آمده و ميتواند نژادها و گونه هاي نزديك را كنترل كند. مثلا" اگروسيناز اگروباكتريوم بوجود آمده و ميتواند نژادها و استرين هاي ديكر را از بين ميبرد. Nopalineو Agrocinopineاختصاصي هستند. Agrocineگروههايي را كه اين اپين ها را توليد ميكنند از بين ميبرد. اينكار با توليد آنتي بيوتيك k-84توسط پلاسميد PAgk84 با 477 kbp وزن، صورت ميگيرد. اگروسين پس از توليد بوسيله آنزيمي بنام Agrocinopine – parmeaseكه بوسيله Ti-plasmidكد ميشود جذب گياه شده و در نتيجه باعث توقف سنتز DNA باكتري ميشود. ( بيماريزايي اگروباكتريوم متوقف ميشود. )
خطر انتقال پلاسميد PAg k84به اگروباكتريومهاي بيماريزا وجود دارد و در نتيجه استرين هاي دريافت كننده، به Agrocineمقاوم ميشوند.
از طريق مهندسي ژنتيك معلوم شده است كه پلاسميد PAgk84 ناحيه اي به نام Tra(15.9kbp)انتقال پلاسميد را كد ميكنند. پس از حذف اين ناحيه ، پلاسميد بدست آمده را PAg k1026ناميدند كه قادر به انتقال اگروسين نبود. از بين دو استرين جديد، PAg k1026و k-84در مبارزه بيولوژيك استفاده كردند. گياهان با استرين هاي بيماريزا آلوده كردند واز اين دو استرين براي مبارزه استفاده كردند. نتايج نشان داد كه هر دو از كنترل بيولوژيك يكساني برخوردار هستند. تعداد گالهاي روي شاهد بيشتر از دوتاي ديگر بود وتوصيه شده است بعلت خطر انتقال پلاسميد و توليد استرين مقاوم از PAgk1026 استفاده شود.
توصيف گونه ي A. radiobacter
مرفولوژي كلني و سلولهاي مشابه مشخصات جنس است.
استرين ها نيازي به عوامل رشد ندارندو روي محيط هاي معدني پايه رشد ميكنند بشرطي كه منبع قابل استفاده كربوئيدرات داشته باشد.
اكثر استرينها از سيترات استفاده ميكنند.
اكثر استرينها از L-تايروزين استفاده نميكنند.
روي محيط New & Kerrرشد نميكنند.
از قندهاي دلسيتول و متيل D گلوكوزيد در محيط آير و همكاران كه داراي 02/0درصد عصاره مخمر است اسيد توليد ميكنند.
از لاكتوز توليد 3 – كتولاكتوز ميكنند.
در º35 رشد ميكنند.
آرجينين دي هيدرلاز مثبت اند ( درمحيط تورنلي )
در محيط فريك آمونيوم ستيرات توليد پوسته ( pellicle) مينمايد . ( برنگ قرمز قهوه اي )
در بسياري از استرينها پلازميد بزرگ Ti يا Ri وجود دارد.
از خاك ، ريزوسفر ، گالهاي جوان و گالريشه ها (hairy roots) ي بسياري از گياهان جدا شده اند.
G+C% در DNAآنها 57 تا 63 % است.
استرين تيپ Atcc19358 = NCIB9042است.
آخرین ویرایش: